Les adénomes hypophysaires sont des tumeurs bénignes originaires de l’hypophyse.
Leur traitement est parfois complexe mais l’évolution est bonne dans la grande majorité des cas.
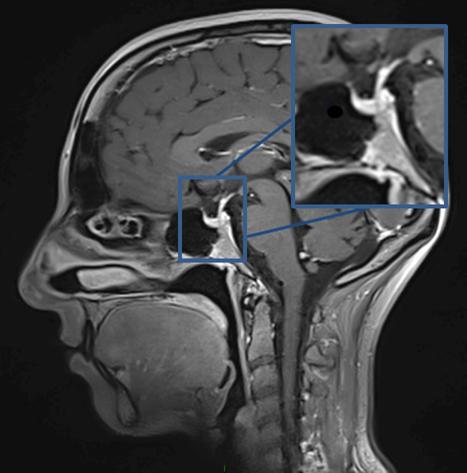
IRM Cérébrale, coupe sagitale : Hypopyse et tige pitutaire.
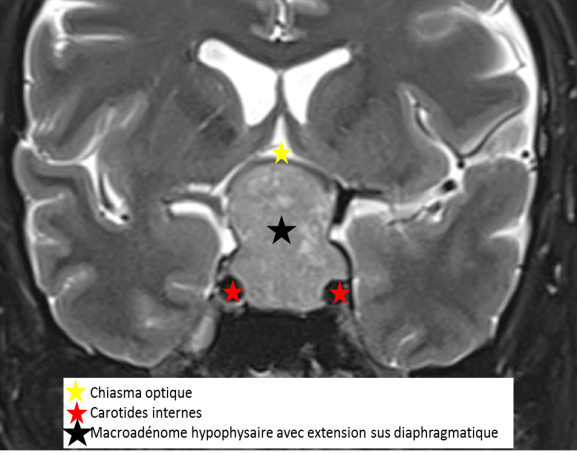
IRM cérébrale, coupe coronale : Macroadénome hypophysaire.
Les adénomes hypophysaires sont souvent découverts de manière fortuite à l’occasion d’une imagerie cérébrale (Scanner ou IRM) faite pour une autre raison.
Les adénomes hypophysaires peuvent entrainer 3 grands types de symptômes en fonction de leur type et de leur taille :
Des symptômes liés à la compression exercée par la tumeur sur les structures avoisinantes :
– Troubles visuels (liés à la compression du chiasma optique situé quelques millimètres au-dessus de l’hypophyse)
• Réduction du champ visuel
• Baisse de l’acuité visuelle
– Céphalées ou maux de tête
– Symptômes liés a la compression des nerfs qui cheminent le long de l’hypophyse dans le sinus caverneux et qui contrôlent les mouvements des yeux. Il s’agit le plus souvent d’une vision double ou d’une chute de la paupière. Ces symptômes sont rares dans les adénomes hypophysaires et signent le plus souvent une nécrose brutale et/ou un saignement dans tumeur.
Des symptômes liés à une sécrétion excessive d’une hormone par la tumeur :
− hypersécrétion de prolactine ou « hyperprolactinémie », responsable d’une disparition des règles (aménorrhée secondaire), d’une sécrétion laiteuse des seins (galactorrhée) ou de troubles sexuels,
− acromégalie secondaire à une hypersécrétion d’hormone de croissance, responsable d’un épaississement progressif et insidieux du visage et des extrémités, d’une hypersudation, d’un syndrome du canal carpien, de douleurs articulaires, d’une hypertension artérielle ou d’un diabète,
− hypercorticisme (syndrome de Cushing) secondaire à une hypersécrétion d’ACTH stimulant la production surrénalienne de cortisol et qui se manifeste par une obésité androïde avec hypertension artérielle, diabète, fatigue, rougeur du visage et parfois des troubles psychiatriques.
− plus rarement, hyperthyroïdie secondaire à une hypersécrétion de TSH par un adénome thyréotrope.
Des symptômes liés a une sécrétion insuffisante de certaines hormones sécrétées normalement par l’hypophyse :
Une réduction ou un défaut de sécrétion des hormones sécrétées normalement pas la partie antérieure de l’hypophyse (hypopituitarisme) se traduit lorsqu’il est global par une fatigue, une pâleur, des troubles sexuels, une peau fine. Le déficit en hormone de croissance chez l’enfant entraîne un retard de croissance. Le déficit en hormone thyroïdienne entraine une pâleur, une prise de poids, une constipation et une dépression. L’insuffisance gonadotrope est lié à un défaut de production des hormones qui stimulent la production d’hormone sexuelle par les ovaires et les testicules. Elle entraine des signes d’hypogonadisme (absence de puberté, aménorrhée, impuissance, infertilité); L’insuffisance corticotrope, la plus dangereuse sur le plan vital, entraîne asthénie, hypotension artérielle et troubles digestifs en cas de décompensation.
Devant ces symptômes, l’analyse clinique permet d’orienter vers une pathologie hypophysaire et en cas de suspicion, un bilan biologique sera réalisé en priorité. Lorsque cette suspicion est confirmée, l’examen radiologique de référence est l’IRM hypophysaire.
Il existe plusieurs sous-types histologiques correspondants aux différents tableaux cliniques:
Les adénomes sécrétants ou fonctionnels
− L’adénome à prolactine (PRL) est le plus fréquent et représente 60% de l’ensemble des adénomes (ratio femme-homme : 10/1, âge moyen au diagnostic de 32 ans)
− L’adénome somatotrope sécrétant l’hormone de croissance (GH) représente environ 13 % de l’ensemble des adénomes ; l’âge au moment du diagnostic est de 47 ans, avec une variante fréquente l’adénome somatoprolactinique, sécrétant de la PRL et de la GH (50% des adénomes somatotropes).
− L’adénome corticotrope est le plus souvent de petite taille (<10mm) ou « micro-adénomes » et sécrète de l’ACTH. Il représente 6% de l’ensemble des adénomes. Les macroadénomes sont moins fréquents.
− L’adénome thyréotrope secrétant la TSH est rare (<1% de l’ensemble des adénomes). Il s’accompagne le plus souvent d’une hyperthyroïdie, mais il peut être silencieux et plurisecrétant (TSH-GH et TSH-PRL).
Les adénomes non sécrétants ou non fonctionnels
Ils représentent 30% des adénomes hypophysaires. Le terme « non fonctionnel » doit être préféré, car dans environ un tiers des cas, il existe une expression hormonale, sans traduction clinique, mais pouvant servir de marqueur biologique. Ces tumeurs sont en majorité des adénomes gonadotropes.
Les adénomes silencieux
Ils sont moins fréquents. Il s’agit d’adénomes se révélant par un syndrome tumoral de compression sans tableau clinique spécifique d’hypersécrétion, mais qui en immunocytochimie sont positifs pour l’ACTH, la GH, ou la TSH voire plurihormonaux (GH et PRL ou TSH et GH). Biologiquement, soit ils ne sécrètent pas d’hormone, soit plus fréquemment, ils sécrètent une pro-hormone inactive expliquant l’absence de signes cliniques ou une hormone en faible quantité, mais dosable (l’hypersécrétion d’ACTH sans hypercorticisme en est l’exemple le plus fréquent).
Les adénomes agressifs ou atypiques et carcinomes
La fréquence des adénomes agressifs est encore méconnue. Seules 0,2% des tumeurs présentent des métastases au cours de l’évolution et sont considérées comme des carcinomes : sécrétants pour la plupart – 36% de PRL, 30% d’ACTH – et non sécrétants dans uniquement 23%. Ces métastases jamais inaugurales surviennent 5 à 16 ans après le début de l’histoire clinique et concernent soit le système nerveux avec une dissémination par le liquide céphalo-rachidien (LCR) soit divers organes: poumons, os, foie voire ganglions lymphatiques.
Qui est concerné ?
Les adénomes hypophysaires représentent entre 10 et 20% des tumeurs intracrâniennes de l’adulte. Ces tumeurs ont une incidence de 4/100 000 habitants avec une tendance à l’augmentation des découvertes fortuites, « incidentalomes ».
Il s’agit d’une tumeur rare (2,7% des tumeurs supratentorielles) chez l’enfant dont la tumeur de la région hypophysaire la plus fréquente est le craniopharyngiome.
Comment fait-on le diagnostic ?
Devant un ensemble de symptômes endocriniens et\ou neurologiques et\ou ophtalmologiques, votre médecin demandera une IRM cérébrale qui confirmera l’existence d’une lésion hypophysaire; il en découlera une consultation avec un neurochirurgien ou un endocrinologue.
Le bilan endocrinien
Le bilan endocrinien sera lancé soit parce que le patient présente un syndrome endocrinien soit parce qu’une lésion de la région hypophysaire aura été découverte en imagerie. Ce bilan comporte de façon routinière le dosage des principaux axes hormonaux (Prolactine ; TSHus ; T4l ; T3l ; FSH ; LH ; Estradiol/ Testostérone ; GH ; Igf1 ; Cortisolémie).
La consultation d’endocrinologie avec le Docteur LALOI-MICHELIN, notre référente, ne sera organisée en préopératoire que dans les cas d’adénomes hypophysaires sécrétants ou devant des insuffisances hormonales sur le bilan. Le cas échéant une substitution hormonale voire un traitement médical de l’adénome secrétant peut être envisagé avant l’intervention.
Le bilan radiologique
L’IRM cérébrale reste l’examen de référence pour explorer les lésions hypophysaires. Cet examen doit être optimal afin d’avoir une description anatomique précise, permettant de définir les limites de l’adénome avec :
- son extension dans la selle turcique
- le diaphragme en haut et l’extension sus diaphragmatique
- les sinus caverneux latéralement,
- la glande hypophysaire saine
- les voies opto-chiasmatiques,
- le diencéphale.
Le scanner cérébral avec un angioscanner en fenêtres osseuses peut être demandée et utilisé en neuronavigation pour guider l’intervention chirurgicale. Cet examen apporte un complément d’information surtout sur l’atteinte osseuse de la loge hypophysaire.
La sémiologie radiologique de la région hypophysaire est très riche et nécessite une bonne expérience du radiologue. Pour cela les dossiers sont revus avec un neuroradiologue référent dans cette pathologie.
Le bilan neuro-radiologique
Le syndrome neuro-ophtalmologique sera exploré en fonction de la plainte visuelle du patient et surtout de l’extension de l’adénome hypophysaire vers les voies opto-chiasmatiques et/ou vers le sinus caverneux sur l’IRM cérébrale. L’examen neuro-ophtalmologique comportera une mesure de l’acuité visuelle, un fond œil et un champ visuel voire un OCT pour apprécier la compression des nerfs optiques, et éventuellement un test de Lancaster si une atteinte des nerfs oculomoteurs est suspectée.
Quels sont les traitements disponibles ?
La prise en charge peut consister en:
- une surveillance neuroradiologique en cas d’adénome non secrétant ;
- un traitement médical dans les adénomes fonctionnels lors qu’existe la possibilité d’un traitement médical antagoniste; dans ce cas, le patient est adressé à un endocrinologue.
- une chirurgie d’exérèse pour les adénomes évolutifs, les adénomes rebelles aux traitements, les adénomes avec une compression des voies opto-chiasmatiques;
- une radiothérapie ou une radiochirurgie pour les adénomes inopérables, les résidus postopératoires dont une reprise chirurgicale est impossible ou à risque important, et les adénomes agressifs.
Le traitement chirurgical
Le neurochirurgien participe à la prise en charge des patients porteurs d’adénomes hypophysaires y compris ceux qui ne nécessitent qu’une surveillance neuro-radiologique. L’adénome hypophysaire est une tumeur bénigne à évolution lente. La surveillance neuro-radiologique permet donc d’en estimer la courbe évolutive et ainsi de ne poser l’indication opératoire que devant une croissance tumorale significative et avant d’avoir une extension importante de l’adénome; une exérèse la plus complète possible sera alors envisagée tout en préservant les fonctions endocriniennes physiologiques de la glande hypophysaire. En cas de microadénome ( < 10 mm), le but de l’intervention chirurgicale est une exérèse complète avec donc une guérison.

Pituitary adenoma
Consultation avec un neurochirurgien
Au cours de cette consultation, un complément de bilan vous sera proposé si nécessaire, la relation entre vos symptômes et la lésion vous seront expliqués ainsi que l’histoire naturelle de ces adénomes et les rapports avec les structures avoisinantes (caractère invasif ou pas de l’adénome). Le neurochirurgien posera éventuellement une indication chirurgicale qui sera faite par voie endoscopique endonasale. La décision d’intervention fait le plus souvent suite à une réunion de concertation pluridisciplinaire pendant laquelle le dossier est discuté en présence des neurochirurgiens, des endocrinologues et des neuroradiologues.
Pourquoi la chirurgie par voie endoscopique endonasale ?
Actuellement, l’immense majorité des adénomes hypophysaires est opérée par voie endoscopique endonasale. Contrairement au microscope, où l’œil du chirurgien reste à l’extérieur du nez, ne donnant qu’une vision très limitée au fond des cavités nasales, l’endoscope emmène l’œil du chirurgien au fond des fosses nasales et permet d’avoir une vue panoramique de la région et de la lésion. Elle permet également grâce à des endoscopes à 30 et 45° de voir latéralement et vers le haut et donc, de mieux apprécier les éventuelles extensions de la tumeur. L’utilisation de voies mini-invasives respectant les cavités nasales, a permis de diminuer significativement la morbidité rhinologique de cette chirurgie et d’augmenter le confort postopératoire des patients.
Consultation et bilan préopératoire
- Bilan radiologique,
- Consultation avec l’endocrinologue si nécessaire,
- Consultation neuro-ophtalmologique si nécessaire,
- Consultation d’anesthésie en cas d’intervention chirurgicale.


